17 Metabolismo do Glicogênio
Objetivos
- Entender o que representa a glicogênese e a glicogenólise, sabendo localizá-las no mapa;
- Compreender como se dá a ativação de glicose-6-P para a síntese do glicogênio;
- Saber as etapas básicas do metabolismo de síntese (ativação/ancoragem, elongamento, ramificação) e de degração do glicogênio; (desramificação/encurtamento, dextrina limite)
- Saber o que é a glicogenina e seu papel na síntese do glicogênio;
- Entender como funciona a glicogênio fosforilase e sua dependência de vitamina B6;
- Compreender o papel da modulação covalente nas enzimas chave do metabolismo do glicogênio;
- Entender o papel do AMP-cíclico para a degradação do glicogênio;
- Saber exemplificar como a fosforilação da glicogênio sintase e da fosforilase atuam em conjunto com outros vias metabólicas de glicose;
- Saber exemplificar alguns controles alostéricos do metabolismo do glicogênio;
- Entender o papel do glicagon e da insulina para o metabolismo do glicogênio.
17.1 Introdução
O glicogênio é a forma animal de armazenamento da glicose. Assim como o amido, é composto exclusivamente de um grande número de glicoses interligadas. Diferentemente daquele, porém, possui muitas ramificações, o que permite armazenar várias glicoses em forma de polissacarídio num espaço bem pequeno. A ramificação do glicogênio se assemelha aos ramos e galhos que saem de um tronco de árvore. Como a glicose serve para produzir energia, estoques de glicogênio são verdadeiras reservas de energia. Eles existem principalmente no fígado e nos músculos.
Quando a célula está precisando de bastante energia, como numa corrida de maratona, esse glicogênio é atacado por diversas enzimas para liberar glicose livre para produção de energia através do metabolismo intermediário. Contrariamente, quando a célula não precisa de grandes quantidades de energia, o que ocorre quando há muitas moléculas de glicose livre no sangue após as refeições, um outro conjunto de enzimas age ligando as moléculas de glicose para estocá-as na forma de glicogênio. O primeiro processo chama-se glicogenólise, ou lise do glicogênio, e o segundo processo, glicogênese, ou síntese de glicogênio. Ambos os processos são estritamente controlados pela célula através de sua disponibilidade de ATP, ou por controle de hormônios, tais como a insulina.
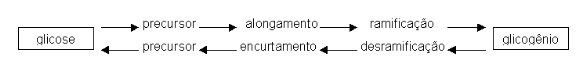
Cuidado para não confundir glicogênese, a produção de glicogênio, com gliconeogênese, a produção de nova glicose a partir de outros compostos. A síntese e degradação de glicogênio envolve reações opostas de enzimas. Na síntese há a formação de uma âncora na qual passa a se encaixar várias moléculas de glicose ligadas entre si, alongando a estrutura, seguida pelas ramificaçãoes. Na degradação, ocorre a quebra dessas ramificações, juntamente com o encurtamento da molécula de glicogênio. No final das contas, pra montar e quebrar o glicogênio, participam umas 6 enzimas diferentes.
17.2 Detalhes
O glicogênio é a forma de armazenamento da glicose. Este armazenamento se faz necessário pois se a glicose existisse livre na célula, o aumento da osmolaridade intracelular seria incompatível com a vida. Não obstante, a mobilização de glicogênio é uma forma rápida de prover glicose ao organismo, diferentemente da gliconeogênese. Estruturalmente, é formado por uma ramificação de moléculas de glicose interligadas, resultando numa polissacarídio de peso molecular aproximado de 105 kD (equivalente a mais de 15 mil moléculas de insulina).
Dependendo das necessidades do organismo, a glicose pode ser então armazenada (síntese de glicogênio, pela glicogênio sintase) ou liberada para oxidação (degradação de glicogênio, pela glicogênio fosforilase). O metabolismo do glicogênio ocorre no citosol hepático (8% do peso do fígado) e muscular (2% do peso do músculo), principalmente. A lógica da via de síntese envolve a produção de um precursor (UDP-glicose), alongamento da cadeia (-Glc-Glc-Glc-), e ramificação. A lógica da via de degradação envolve um encurtamento da cadeia simultâneo à desramificação, e conversão à glicose-6-P. A mobilização do glicogênio muscular é pouco afetada no jejum, a não ser em casos extremos. Entretanto, é a principal fonte de energia do músculo em repouso quando este inicia uma atividade, exaurindo seus estoques em 8 a 12 min.
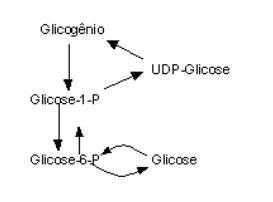
No metabolismo de síntese e degradação do glicogênio estão envolvidas uma dúzia de enzimas. A síntese se inicia por uma glicomutase (Glc-6-P -> Glc-1-P) que prepara a glicose para sua ativação ao UDP, ação efetivada pela UDP-Glc-pirofosforilase, e resultando em UDP-Glc. A partir desta, ligações
A degradação do glicogênio inicia-se simultaneamente através de sua desramificação e encurtamento pela glicogênio fosforilase, que remove resíduos de glicose nas ligações
A ação da glicogênio fosforilase ocorre até o ponto limite de 4 resíduos de glicose, quer nos ramos (dextrina limite) ou no esqueleto principal do glicogênio. A regulação de síntese e degradação de glicogênio ocorre principalmente por modulação das atividades da glicogênio sintase (ativada por glicose-6-P da dieta, e por ATP; inibida por c-AMP e glicagon) e da glicogênio fosforilase (ativada por c-AMP, Ca2+; inibida por insulina).
17.3 Aplicação
O glicogênio representa de 2 a 8% do peso úmido do fígado, e até 1% do tecido muscular. Normalmente é determinado na bromatologia de carcaças, à excessão da de peixes, onde exerce uma contribuição inferior a 1 %. Porém, em moluscos (ostra, mexilhão), o glicogênio pode atingir até 10 % da matéria seca do pescado. Assim, para a diferenciação de espécies de peixes em geral, são empregados métodos de determinação de lipídios.
Na produtividade animal, 70-90% da glicose mobilizada pelo glicogênio e pela gliconeogênese é utilizada na elaboração do leite, cujo açúcar principal, a lactose, é formada por ligação de galactose com glicose. Dessa forma, contém o leite até 90 vezes mais açúcar que o sangue. A necessidade de glicose em ruminantes oscila entre 30 a 60 mg/dL de sangue (metade da de humanos e monogástricos), com o sistema nervoso fazendo uso de 15% desta.
A maior demanda da glicose ocorre no final da prenhez e lactação animal. As fontes de glicose em monogástricos inclui o amido e a sacarose; em poligástricos, soma-se a estas a celulose, a qual é levemente convertida pela fermentação ruminal.
17.3.1 Doenças
As doenças do metabolismo do glicogênio são severas, já que lidam com estocagem e fonte de energia organismal. Assim, a doença de Von Gierke, que afeta o fígado, rins e intestino, e é ocasionada por deficiência da glicose-6-fosfatase, leva a uma esteatose, hiperacidemia lática, hepatomegalia e hipoglicemia severas.
A doença de Pompe, por sua vez, age contrariamente, no acúmulo lisossômico de glicogênio produzido por deficiência da
Síntese
- Conceito: síntese e degradação, tendo a glicose como unidade formadora;
- Importância: armazenamento (síntese) e provimento (degradação) de glicose, dependendo das necessidades do organismo;
- Localização: citosol hepático e muscular, principamente
- Lógica da via de síntese: síntese de precursor (UDP-glicose), alongamento da cadeia (Glc-Glc-Glc-etc) e ramificação;
- Lógica da via de degradação: encurtamento da cadeia e desramificação simultâneos, e conversão a glicose-6-P;
- Regulação da degradação: saciedade (+), cálcio (+), insulina (-);
- Doenças: doença de von Gierke (deficiência da glicose-6-fosfatase, levando a esteatose e hipoglicemia severa); doença de Andersen (deficiência na enzima desramificadora, levando a cirrose hepática infantil progressiva e morte); doença de Pompe (acúmulo de glicogênio nos vacúolos lisossômicos por deficiêncie de -1,4-glicosidade, ocasionando a doença de depósito de glicogênio tipo II).