12 Glicólise
Objetivos
- Localizar a Glicólise no Mapa Metabólico;
- Entender a lógica da via glicolítica em anaerobiose;
- Identificar os produtos principais da glicólise (ATP e piruvato);
- Saber diferenciar energeticamente a glicólise anaeróbia da aeróbia;
- Saber estimar o rendimento energético percentual do processo (~40%);
- Entender em qual compartimento celular ocorre a glicólise anaeróbia;
- Saber diferenciar a fermentação lática da alcoólica
- Identificar no Mapa alguns pontos críticos da via glicolítica (investimento e resgate de ATP), e como é modulada (inibida, ativada);
- Identificar no Mapa o ponto de bifurcação que produz dois C3 a partir de um C6, enzima que opera e coenzima envolvida (clivagem aldólica);
- Identificar suas etapas chave e respectivas enzimas (hexoquinase, fosfofrutoquinase e piruvato quinase);
- Compreender como a glicose é transportada para a célula;
- Saber qual o saldo líquido energético da fermentação glicolítica;
- Entender como a glicólise anaeróbia é controlada (oferta de S, e modulações alostérica, covalente e neuroendócrina);
- Entender que a via é essencialmente ativada ou inibida pela necessidade ou não de ATP à célula, respectivamente;
- Identificar no Mapa os destinos principais do piruvato;
- Perceber quais vitaminas são necessárias para o correto funcionamento da via;
- Saber exemplificar algumas situações e bloqueio da via metabólica, tais como inibidores naturais e patogenias gerais;
- Saber equacionar a glicólise, com substratos (ADP, Pi, NAD+, glicose) e produtos correlatos;
- Compreender a importância de compostos ativadores da glicólise, tais como Fru-2,6-bifosfato.
12.1 Introdução
A glicólise inicia um capítulo da bioquímica denominado de metabolismo intermediário. Chama-se intermediário pois existe em praticamente todo o organismo vivo, e compõe-se da glicólise, ciclo de Krebs e cadeia respiratória. A glicólise existe virtualmente em toda célula ou bactéria conhecida. Já o ciclo de Krebs e a cadeia respiratória, apenas nas que possuem mitocôndrias ou cloroplastos. A glicólise tem esse nome devido à sua origem latina, onde glycos quer dizer açúcar, e lysis, quebra. Portanto, a glicólise é a via de quebra do açúcar. Mas pra quê quebrar moléculas de açúcar ? Pra produzir energia. Assim como um automóvel queima gasolina para se locomover, as células queimam o açúcar para cumprir suas funções biológicas.
Dessa forma, o objetivo da glicólise é pegar o açúcar ingerido pela dieta e transformá-lo em energia. Essa energia não está solta no ar, mas sim contida em moléculas especiais. A molécula mais utilizada por todo o organismo para supri-lo de energia, considerada “a moeda energética” dos seres vivos é o ATP. A quebra de ATP libera energia suficiente para cumprir um número infindável de operações metabólicas. Resumindo: a glicólise existe pra fazer ATP. A glicólise também é chamada de fermentação. Em poucas palavras, trata-se de uma via metabólica que produz ATP sem precisar de oxigênio. Neste sentido, bactérias que fazem iogurte, células musculares em atividade vigorosa, e a microbiota do intestino grosso, sobrevivem graças ao ATP que elas fabricam por fermentação. Assim como em toda a rota do metabolismo, animal, vegetal, ou microbiano, a química que faz com que o açúcar da glicose se transforme em ATP energético envolve um grande número de proteínas com funções especiais, as enzimas.
Existem 10 enzimas especiais na glicólise, correspondentes aos 10 passos necessários para quebrar uma molécula de glicose, produzindo ATP energético e outros compostos importantes para o metabolismo, como o piruvato e o lactato. Para a glicólise funcionar direito, precisa-se das enzimas, de glicose, de algumas vitaminas e minerais, e de colaboradores das enzimas, as coenzimas. Se houver algum problema com quaisquer dessas enzimas ou compostos, o ATP não é formado, o que pode resultar numa baixa de energia no organismo. Mais grave ainda, para as células que dependem exclusivamente desta rota metabólica para sobreviver, como bactérias de fermentação e hemácias, sua destruição.
12.2 Detalhes
Glicólise é a via de oxidação da glicose para a produção de energia, com saldo de duas moléculas de ATP, e para a síntese de precursores de outras vias metabólicas, como NADH, piruvato e acetil CoA. Ocorre no citosol e distingue-se quando da presença de O2 (glicólise aeróbica, permite o funcionamento do ciclo de Krebs e da cadeia respiratória) ou de sua ausência/insuficiência (glicose anaeróbica, com produção de etanol ou lactato). Neste caso, o NADH produzido é utilizado para a produção de ácido lático, zerando o saldo desta coenzima.
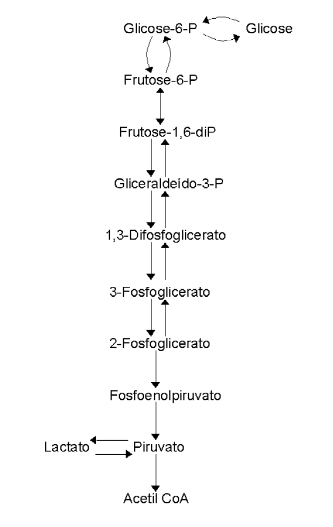
Cérebro e hemácias constituem sítios nos quais a glicólise é imprescindível. A lógica da via envolve um aprisionamento celular (fosforilação da glicose), investimento energético (consumo de 2 ATPs), clivagem de composto C6 em dois C3, e resgate energético de 2 ATPs em cada ramo do metabolismo de C3 (total: 4 ATP; gasto: 2 ATP; saldo: 2ATP, vide figura). A glicólise se inicia com o transporte (facilitado ou co-transporte) de glicose às células, ao que se sucede uma fosforilação diferencial da molécula. No fígado, essa fosforilação é conduzida pela glicoquinase, enzima específica para a glicose, com uma reação de alto Km, ao passo que nos demais tecidos a fosforilação é conduzida pela hexoquinase, enzima de baixo Km, e que também fosforila outras hexoses.
A glicólise é essencialmente controlada em suas 3 etapas irreversíveis, realizadas pela hexoquinase, fosfofrutoquinase (fornece à molécula isomerizada em frutose, uma simetria C6 que permite sua posterior clivagem pela aldolase em 2 C3), e piruvato quinase (última etapa, com produção de ATP). À luz do controle hormonal, pode-se afirmar que a insulina (hormônio da saciedade) age positivamente na via glicolítica, ao passo que o glicagon (hormônio da fome) a inibe. Além destes, teores aumentados de frutose-2,6-difosfato, frutose-1,6-difosfato e 2,3-difosfoglicerato (o 2,3-DPG presente nas hemácias) também atuam positivamente na glicólise.
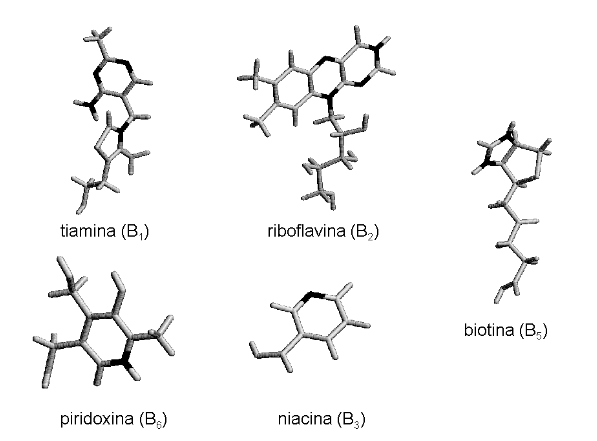
De modo geral, a presença desses compostos sinalizam para um catabolismo do qual a glicólise faz parte. Excesso de citrato, por sua vez, inibe a via glicolítica. Para a produção de ATP em dois eventos da via glicolítica, é necessário a síntese de compostos intermediários de alta energia, quais sejam, o 1,3-difosfoglicerato e o fosfoenolpiruvato, que precedem a liberação de ATP. Vitaminas B1 (tiamina), B2 (riboflavina) e niacina são necessárias à atuação de algumas enzimas da glicólise.
12.3 Aplicação
A glicólise é essencialmente controlada em suas 3 etapas irreversíveis, realizadas pela hexoquinase, fosfofrutoquinase (fornece à molécula isomerizada em frutose, uma simetria C6 que permite sua posterior clivagem pela aldolase em 2 C3), e piruvato quinase (última etapa, com produção de ATP). À luz do controle hormonal, pode-se afirmar que a insulina (hormônio da saciedade) age positivamente na via glicolítica, ao passo que o glicagon (hormônio da fome) a inibe. Além destes, teores aumentados de frutose-2,6-difosfato, frutose-1,6-difosfato e 2,3-difosfoglicerato (o 2,3-DPG presente nas hemácias) também atuam positivamente na glicólise.
De modo geral, a presença desses compostos sinalizam para um catabolismo do qual a glicólise faz parte. Excesso de citrato, por sua vez, inibe a via glicolítica. Para a produção de ATP em dois eventos da via glicolítica, é necessário a síntese de compostos intermediários de alta energia, quais sejam, o 1,3-difosfoglicerato e o fosfoenolpiruvato, que precedem a liberação de ATP. Vitaminas B1 (tiamina), B2 (riboflavina) e niacina são necessárias à atuação de algumas enzimas da glicólise.
A excreção renal de glicose oscila entre diversos animais: enquanto que a galinha excreta até 170 mg/dL de glicose em sua urina, o cão e o cavalo excretam 70 mg/dL, e o boi, 45 mg/dL.
A interrupção da glicólise pode ocorrer com o uso de diversas drogas ou pelo consumo de plantas tóxicas. Neste sentido, a cavalinha (Equisetum pyramidale) possui princípios tóxicos que reduzem o teor de vitamina B1 e aumentam o de piruvato. Por consequência, o animal sofre perda na produção de leite e no controle muscular. A administração de flúor à água potável tem por função a inibição de bactérias anaeróbicas que crescem abaixo da superfície da placa de polissacarídios do esmalte dentário, interrompendo a produção de ácido lático e pirúvico das mesmas, destruidores da superfície esmaltada.
A glicólise também tem sua importância generalizada no tecido vegetal, à excessão dos cloroplastos, que produzem ATP por reação fotoquímica, não dependendo portanto da via glicolítica para esse fim. Na verdade, não existe nessas organelas, o arsenal enzimático completo para operar a via glicolítica ou o ciclo de Krebs, tornando estas duas vias pouco funcionais para o mesmo.
12.3.1 Aspectos clínicos
Algumas drogas são conhecidas inibir a via glicolítica, como a iodoacetamida e o fluoroacetato (inibição da gliceraldeído-P-desigrogenase), arsenatos e fluoretos (inibição da enolase). Estas interrupções promovem uma inativação da via, e consequente estagnação do metabolismo intermediário.
A administração de flúor à água potável tem por função a inibição de bactérias anaeróbicas que crescem abaixo da superfície da placa de polissacarídios do esmalte dentário, interrompendo a produção de ácido lático e pirúvico das mesmas, ambos destruidores da superfície esmaltada. Algumas doenças conhecidas da glicólise incluem a anemia hemolítica eritrocitária (deficiência da piruvato quinase), a síndrome alcoólica fetal (oxidação de etanol a acetaldeído requer NAD+, que também é requisitado pela glicólise), a deficiência da piruvato desidrogenase (com consequente acidose lática provocada pelo acúmulo de piruvato e alanina), e a deficiência da glicose fosfato isomerase.
A glicólise anaeróbica também é utilizada pelo organismo frente a demandas diminuidas de oxigênio, como no infarto do miocárdio, embolia pulmonar e hemorragia descontrolada. Neste caso, o teor de lactato sanguíneo fornece rápida informação a respeito do débito de oxigênio do paciente, o excesso de oxigênio necessário para a recuperação de um período em que sua disponibilidade foi inadequada.
 ### Síntese {.unnumbered}
### Síntese {.unnumbered}
- Conceito: via de oxidação da glicose;
- Importância: síntese de ATP (2), e precursores de outras vias (piruvato e acetil CoA);
- Localização: citosol;
- Distinção: glicose aeróbica (presença de O2 permite funcionamento do ciclo de Krebs e da cadeia respiratória) X anaeróbica (produção de etanol ou lactato, pela insuficiência/ausência de O2);
- Tecidos em que a via é imprescindível (hemácias, cérebro);
- Lógica da via: aprisionamento celular (fosforilação da glicose), investimento energético (gasto de 2 ATPs), clivagem de C6 em dois C3, e resgate energético de 2 ATPs em cada ramo (total: 4 ATPs; gasto: 2 ATPs; saldo: 2 ATPs);
- Etapa inicial: transporte de glicose às células (transporte facilitado e co-transporte);
- Etapas irreversíveis: hexoquinase, fosfofrutoquinase e piruvato quinase;
- Importânica da gliceraldeído-3P-desidrogenase e da enolase;
- Diferenças na fosforilação da glicose: hexoquinase (tecidual, baixo Km) e glicoquinase (hepática, alto Km);
- Clivagem: uma glicose formando dois piruvatos (aldolase);
- Metabólitos envolvidos no controle glicolítico: ação de frutose 2,6-difosfato, frutose 1,6-difosfato, e 2,3-difosfoglicerato;
- Efeito de drogas: iodoacetamida e fluoroacetato (inibição da gliceraldeído 3P desidrogenase) e arsenatos (inibição da enolase); esta interrupção promove a inativação da via, e consequente estagnação do metabolismo intermediário;
- Intermediários de alta energia (precedente à formação de ATP): 1,3-difosfoglicerato e fosfoenolpiruvato;
- Principais vitaminas da via: niacina e vit B1;
- Doenças: anemia hemolítica eritrocitária (deficiência de piruvato quinase) e síndrome alcoólica fetal;
- Regulação: insulina (+) e glucagon (-);
- Destino anaeróbico: na ausência de O2, o NADH produzido durante a fase de investimento é utilizado para a produção de ácido lático, zerando o saldo desta coenzima.