29 Insulina e Glicagon
29.1 Introdução
A comunicação entre as células de mamíferos superiores se dá através de neurotransmissores e de hormônios. Desses últimos, os mais importantes na regência do mapa metabólico nos diferentes tecidos são a insulina e o glicagon. Ambos são hormônios peptídicos, o que significa que são formados por aminoácidos. Em poucas palavras, a insulina é o hormônio da saciedade, enquanto que o glicagon é o hormônio da fome. Isto significa que a insulina age sempre de maneira contrária a do glicagon. Quando se pega o mapa metabólico, verifica-se que algumas rotas servem pra produzir açúcares, proteínas e gorduras, enquanto que outras servem justamente para o oposto, ou seja, quebrar açúcares, proteínas e gorduras.
Sendo assim, quando o organismo precisa de energia, ele aciona as rotas metabólicas que quebram fontes de energia para produzir ATP, ao passo que, quando o organismo não precisa de mais energia, encontrando-se bem alimentado, ele usa os nutrientes da dieta para construir as novas fontes de energia que poderão ser utilizadas quando o ATP estiver faltando. E é aí que entram os papéis da insulina e do glicagon. A insulina vai agir sempre que o organismo estiver saciado, aumentando a absorção de açúcares, aminoácidos e ácidos graxos, no intestino, para a produção respectiva de glicogênio, proteínas e triacilglicerol, fontes primárias de energia no organismo.
Quando o organismo estiver com fome, precisando manter os níveis de glicose sanguínea estáveis para as células, sem contudo injerir nenhum alimento (como antes do café da manhã, do almoço e do jantar), ele aumenta a produção do glicagon, que vai agir no sentido de se produzir glicose para manter o nível sanguíneo desta para uso celular. Neste sentido, o glicagon vai estimular a quebra do glicogênio para liberar glicose, a transformação de aminoácidos e outros produtos em glicose, e a quebra dos triglicérides, que vão liberar o glicerol de suas estruturas para que este também se transforme em glicose.
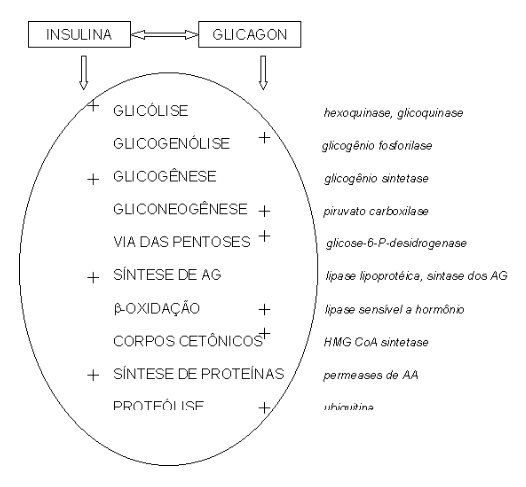
Falando um pouco mais tecnicamente, a insulina vai ativar as rotas de construção (anabolismo), que são a síntese de proteínas, a lipogênese (síntese de ácidos graxos), a glicogenogênese (síntese de glicogênio) e a glicólise (quebra de glicose pra produzir ATP).
Contrariamente, o glicagon, por sua vez, vai atuar ativando as rotas de quebra (catabolismo), as quais são a proteólise (quebra de proteínas), a lipólise (quebra de ácidos graxos, também chamada de \(\beta\)-oxidação), a glicogenólise (quebra do glicogênio), a gliconeogênese (síntese de nova glicose a partir de outros produtos do metabolismo), a via das pentoses (para produzir açúcares que poderão se transformar em glicose), e a cetogênese (produção de corpos cetônicos, ácidos orgânicos que podem ser utilizados pelo organismo para produzir energia).
29.2 Detalhes
A comunicação celular se dá através do trinômio hormônios-sistema nervoso-substratos circulantes. Neste sentido, a integração do metabolismo energético se dá através dos hormônios peptídicos insulina e glicagon, e das catecolaminas de ação neurológica, epinefrina e norepinefrina. Este texto decorre sobre os dois hormônios: insulina e glicagon.
29.2.1 Síntese de insulina
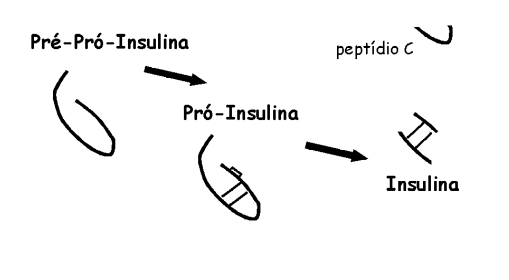
A insulina é um hormônio polipeptídico de efeitos anabólicos (hormônio da saciedade), produzido pelas células \(\beta\) das ilhotas pancreáticas. A insulina é sintetizada como pré-pró-insulina (sequência sinal), sofre transformações, como perda da sequência sinalizadora no RER, tornando-se pró-insulina. Posteriormente, a pró-insulina sofre clivagem peptídica (Golgi), gerando a insulina, um hormônio de duas cadeias contendo 51 aminoácidos totais, e com 3 pontes dissulfeto (duas intercadeia).
Existem variações na sequência de aminoácidos da insulina entre as espécies. A insulina suína difere da humana pela substituição única de Ala desta por Thr. Tal alteração faz com que a administração humana de insulina porcina tenha efeitos indesejáveis, tais como menor tempo de duração do efeito, maior tempo de absorção, e episódios de rejeição. A lógica da ação insulínica é a de exaurir glicose do plasma. Sendo assim, a secreção de insulina é estimulada por glicose, aminoácidos, hormônios gastrointestinais (secretina), e glicagon. Contrariamente, sua secreção é inibida por epinefrina (trauma, estresse) e escassez de combustíveis orgânicos.
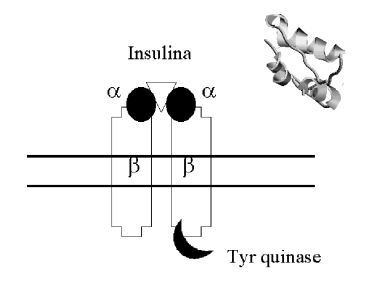
Os efeitos metabólicos da insulina ocorrem no metabolismo de carboidratos, lipídeos e proteínas. No metabolismo de carboidratos a insulina inibe a gliconeogênese e glicogenólise hepáticas, ativa a glicogênese hepática e muscular, e age no aumento da síntese de transportadores de glicose em músculo e hepatócitos. No metabolismo lipídico, a insulina inibe a -oxidação por defosforilação da lipase sensível a hormônio, e aumenta a síntese de ácidos graxos, por aumento de glicerol-3-P e lipase lipoprotéica. A síntese de proteínas também aumenta com insulina. O mecanismo de ação da insulina é complexo, envolvendo uma ligação inicial da macromolécula ao seu receptor transmembrânico, o que permite uma ativação do domínio de tirosina quinase do mesmo. Este domínio promove uma auto-fosforilação em resíduos de tirosina do mesmo (posteriormente fosforiladas por outras proteínas, após algumas horas), em uma reação em cascata (mediada por baixos teores de c-AMP) que culmina com o aumento e externalização de transportadores de glicose (segundos), modificações alostéricas em proteínas (horas), e síntese de DNA e enzimas correlatas (dias). Algumas células são insensíveis à insulina, como o sistema nervoso, mucosa intestinal, túbulos renais e córnea.
O glicagon é hormônio polipeptídico de efeitos catabólicos (hormônio da fome), e secretado pelas células das ilhotas pancreáticas. O glicagon atua em conjunto com epinefrina, cortisol e hormônio de crescimento, GH (hormônios contra-regulatórios). O glicagon é secretado como um precursor de alto peso molecular, sofrendo, como a insulina, uma série de clivagens proteolíticas até sua conformação final. Contrariamente à insulina, não são conhecidas variantes de aminoácidos no glicagon, entre mamíferos. O glicagon, como hormônio da fome, previne contra a hipoglicemia transitória comum aos mamíferos. O glicagon é positivamente regulado por baixa glicemia, aminoácidos da dieta, e epinefrina. Alta glicemia inibe a secreção de glicagon Os efeitos metabólicos do glicagon são antagônicos aos da insulina. Sendo assim, este hormônio aumenta a glicogenólise hepática e gliconeogênese do metabolismo de carboidratos, aumenta a liberação de ácidos graxos e formação de corpos cetônicos dos lipídeos, e aumenta a captação de aminoácidos para a gliconeogênese.
O mecanismo de ação do glicagon inicia com sua ligação ao receptor, ativação de adenilato ciclase, aumento de c-AMP, e forsforilações/defosforilações subsequentes de enzimas e proteínas. O glicagon previne contra a hipoglicemia, quando os níveis de glicose atinge valores inferiores a 45mg/dl de sangue (normoglicemia: 90-110mg/dl). Nesta situação, podem ser identificados sintomas adrenérgicos, como sudorese, palpitação, e tremor, ou sintomas neuroglicopênicos, com celaféia, convulsões e morte.
A glicoregulação se dá através da atividade das células \(\beta\) das ilhotas, de glicoreceptores hipotalâmicos e de hormônios hipofisários, como ACTH, GH, ou contra-regulatórios. Os episódios hipoglicêmicos podem ser de caráter transitório, como o pós-prandial, de jejum (sintomas neuroglicopênicos, lesão hepatocelular, insuficiência adrenal), ou por intoxicação alcoólica (excesso de NADH desvia a rota gliconeogênica, por redução de oxalacetato em malato, e de piruvato em lactato).
Síntese
- Comunicação celular: trinômio hormônios-sist. nervoso-substratos circulantes;
- Integração do metabolismo energético: insulina, glicagon, epinefrina, norepinefrina, catecolaminas;
29.2.1.1 Insulina
- Conceito: hormônio polipeptídico de efeitos anabólicos (hormônio da saciedade), produzido pelas células \(\beta\) das ilhotas pancreáticas;
- Síntese: sintetizado como pré-pró insulina (sequência sinal), sofre transformações como perda da sequência sinalizadora no RER, tornando-se pró-insulina e, posteriormente, clivagem peptídica (Golgi), gerando a insulina, um hormônio de duas cadeias contendo 51 aminoácidos totais, e com três ligações dissulfeto;
- Variações da insulina (humana): insulina suína (difere na substituição de Ala por Thr), e insulina bovina (difere em três aminoácidos); o emprego da insulina porcina é utilizado em humanos, mas com resultados indesejáveis, tais como menor duração do efeito, maior tempo de absorção e episódios de rejeição;
- Regulação da insulina (a idéia é exaurir a glicose do plasma): estímulo por glicose, aminonácidos, hormônios gastrintestinais (secretina) e glicagon; inibição por epinefrina (trauma, estresse), e escassez de combustíveis;
- Efeitos metabólicos da insulina; carboidratos: inibição de gliconeogênese e glicogenólise (fígado), aumento da neoglicogênese (fígado e músculo), aumento de síntese de transportadores de glicose (músculo e adipócitos); lipídios: inibição da oxidação (defosforilação da lipase sensivel a hormônio), aumento da síntese de ácidos graxos (aumento de glicerol-3-P e lipase lipoprotéica); proteínas: aumento de síntese
- Mecanismo de ação da insulina: ligação de insulina ao receptor transmembrânico ativa domínio de tirosina quinase, promovendo autofosforilação e fosforilação de outras proteínas (horas), em reação em cascata, bem como aumento e externalização de transportadores de glicose (segundos), e síntese de DNA e enzimas correlatas (dias);
- Tecidos insulino-independentes: hepatócitos, eritrócitos e células do sist. nervoso, mucosa intestinal, túbulos renais e córnea;
29.2.1.2 Glicagon
- Conceito: hormônio polipeptídico de efeitos catabólicos (hormônio da fome) secretado pelas células α das ilhotas pancreáticas, agindo em conjunto com epinefrina, cortisol e homônio de crescimento (hormônios contra-regulatórios);
- Síntese: secretado como precursor de alto peso molecular, o glicagon sofre uma série de clivagens proteolícas até sua conformação final; não existem variantes nos mamíferos;
- Regulação do glicagon (prevenção de hipoglicemia): estímulo por baixa glicemia, aminoácidos da dieta, epinefrina; inibição por alta glicemia;
- Efeitos metabólicos do glicagon: carboidratos - aumento da glicogenólise hepática e neoglicogênese; lipídios: aumento de liberação de ácidos graxos e corpos cetônicos; proteínas: aumento de captação de aminoácidos para a gliconeogênese;
- Mecanismo de ação do glicagon: ligação ao receptor, ativação de adenilato ciclase, aumento de AMPc e fosforilações/defosforilações subsequentes, em cascata12. Hipoglicemia (glicemia inferior a 45mg/dL); sintomas: adrenérgicos (sudorese, palpitação, tremor) e neuroglicopênicos (cefaléia, convulsões, morte);
- Glicoregulação: células \(\alpha\) das ilhotas, glicoreceptores hipotalâmicos e hormônios, como ACTH e GH hipofisários, bem como contra-regulatórios;
- Tipos de hipoglicemia: pós-prandial (transitória), de jejum (sintomas neuroglicopênicos, lesão hepatocelular, insuficiência adrenal), e por intoxicação alcoólica (excesso de NADH desvia a rota gliconeogênica, por redução de oxalacetato em malato, e de piruvato em lactato).