15 Gliconeogênese
Objetivos
- Entender pra que serve a gliconeogênese e a razão deste termo;
- Saber quais etapas são revertidas à síntese de glicose na via glicolítica, pela gliconeogênese;
- Entender a importância da biotina como vitamina hidrossolúvel no processo;
- Entender a importâncias de suas enzimas-chave, piruvato carboxilase, PEP-carboxiquinase, frutose-1,6-bifosfatase, e glicose-6-fosfatase;
- Localizar a gliconeogênese no mapa metabólico, bem como seus atores (compostos e enzimas principais);
- Saber o motivo pelo qual os músculos não operam a gliconeogênese;
- Entender como o oxalacetato mitocondrial surge metabolicamente no citoplasma para a gliconeogênese;
- Saber do impacto negativo de insulina e avidina para a rota;
- Entender porque a rota é altamente custosa, com 12 ATPs sendo consumidos para a síntese de glicose;
- Entender para que serve e como funciona o ciclo de Cori;
- Entender como a rota é modulada por glicagon na atividade de frutose-1,6-bifosfatase/fosfofrutoquinase.
15.1 Introdução
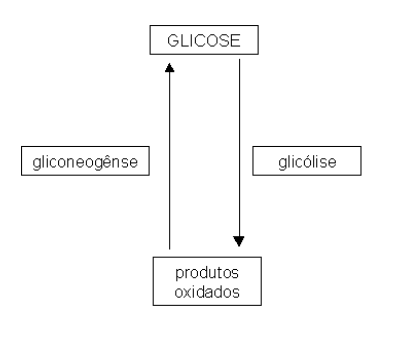
Apesar do nome pomposo, a gliconeogênese nada mais é do que uma re-síntese de glicose. Enquanto que a glicólise quebra a molécula de glicose, a gliconeogênese a constrói novamente. Só isso. Mas pra quê fazer glicose ? Acontece que existem situações especiais no organismo em que é preciso sintetizar a glicose para que a mesma seja utilizada pelos tecidos. Um exemplo: quando se acaba de comer, os nutrimentos vão sendo trabalhados pelo organismo para produzir energia. Parte dessa energia é utilizada, com o excedente sendo estocado para uso posterior, quando a célula precisar.
Essa energia estocável se dá na forma de gorduras e de glicogênio (ou amido, se você for uma batata!). Como o glicogênio é feito de várias moléculas de glicose ligadas, tchan, tchan, tchan, tchan! Produtos oxidados e em excesso no metabolismo podem se transformar novamente em glicose, para armazenamento. Mas por quê não denominar essa produção nova de glicose de glicogênese ?
Bom, aí é por dois motivos. Primeiramente, glicogênese tem a ver com a produção do glicogênio, e não da glicose. Mas o motivo mais relevante é que essa nova produção de glicose não passa pelo mesmo caminho que a sua quebra, a glicólise. Caprichos do metabolismo. Então, puseram o nome de glico+neo+gênese. Outra situação muito comum em que ocorre a gliconeogênese é quando o organismo precisa de glicose a todo o custo, como por exemplo no trabalho do cérebro. Neste caso, alguns compostos ácidos costumam virar glicose. A cãimbra, que também é produzida por um acúmulo de ácido nos tecidos, desaparece lentamente graças a essa maravilhosa rota metabólica, que elimina os ácidos dos tecidos.
15.2 Detalhes
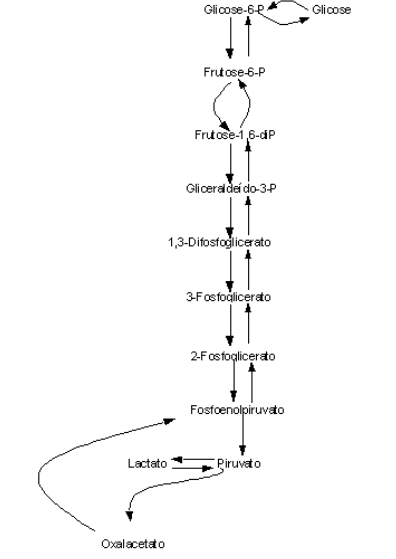
A gliconeogênese é a uma rota metabólica para a síntese de novo de glicose a partir de seus derivados oxidados, tais como piruvato e lactato. Localizada no citosol, principalmente hepático, figura-se de vital importância na manutenção da glicemia e na eliminação do ácido lático pelo organismo. A lógica da via envolve um contorno da última conversão irreversível da glicólise (fosfoenolpiruvato -> piruvato), e produção de glicose através de um reverso da via glicolítica. As fontes primárias para a re-síntese de glicose incluem propionato (principal fonte a partir de gorduras de número ímpar de carbonos), proteínas (20-50%, Ala e Gln, principalmente), glicerol, lactato e alfa-cetoácidos.
Durante o processo ocorre consumo de 2 NADH, 2 GTP e 6 ATP, para cada molécula de glicose sintetizada. A via gliconeogênica se inicia com um desvio de rota do piruvato para oxalacetato, pela piruvato carboxilase, enzima que emprega a vitamina biotina, particularmente presente em fígado, leite e gema de ovo, para a carboxilação do piruvato à oxalacetato (consumo de 1 ATP). Como este último encontra-se na matriz mitocondrial, é necessário uma conversão deste em malato, o qual pode atravessar a membrana da mitocôndria, seguida da regeneração de oxalacetato na citosol. Esta etapa ocorre com consumo e liberação de 1 NADH, sendo, portanto, de saldo líquido nulo para este último.
Uma vez transportado, o oxalacetato é transformado em fosfoenolpiruvato pela PEP-carboxiquinase citosólica, com consumo de 1 GTP e liberação de 1 CO2. A partir desta etapa, a rota gliconeogênica se assemelha a uma reversão da glicolítica, apenas se diferenciando nas enzimas das etapas irreversíveis desta, a saber, a hidrólise de frutose-1,6-di-P pela frutose-1,6-difosfatase, e a defosforilação da glicose-6-P pela glicose-6-fosfatase, liberando glicose. Em suma, para reverter as 3 operações irreversíveis da glicólise, são necessárias 4 reações distintas. Estas, assim como aquelas, estão sob rígido controle do metabolismo. Assim, a presença do modificador alostérico frutose-2.6-di-P, bem como níveis elevados de AMP, inibem a atuação da frutose-1,6-difosfatase do fígado e rins. Além disso, a glicose-6-fosfatase, assim como a piruvato carboxilase, ocorre nestes dois orgãos, mas não no músculo. Dessa forma, o músculo não pode fornecer glicose para a gliconeogênese. O glicagon, por sua vez, ativa a gliconeogênese, através da redução do modificador alostérico frutose-2,6-diP.
Este mecanismo envolve uma interação do hormônio com seu receptor de membrana, produção de c-AMP, aumento de proteína quinase A, e consequente fosforilação e inativação da fosfofrutoquinase-2, que produz a frutose-2-6-diP, reduzindo a inibição da frutose-1,6-difosfatase da gliconeogênese. A gliconeogênese possui ainda um importante ciclo para a eliminação do ácido lático, responsável por acidose metabólica, paralisia muscular e cãimbra: o ciclo de Cori. Nesta rota cíclica, a glicose originária do sangue é convertida pelo músculo em exercício em lactato ou Ala, que se difundem no sangue. Este produtos do metabolismo podem ser captadoa pelo fígado e convertidos em glicose, a qual é liberada novamente na circulação.
15.3 Aplicação
Das enfermidades conhecidas da rota da gliconeogênese destaca-se a hipertermia maligna, que pode ser induzida por megadosagens de aspirina, e que é causada por um aumento nos processos termogerados que resultam em quadro de acidose metabólica e rigidez muscular. Esta moléstia pode também ser causada por halotano, um anestésico termogerador que aumenta a atividade da frutose-1,6-difosfatase e de canais de Ca2+.
O alcoolismo também influencia a gliconeogênese, gerando hipoglicemia, uma vez que que o álcool inibe a via pelo excesso de NADH produzido na conversão de etanol em acetaldeído. Este excesso bloqueia a conversão de lactato em glicose e promove a conversão de Ala em lactato, ambos os processos culminando no aumento do teor final deste (acidose metabólica), e na inibição da re-síntese de glicose.
Hipoglicemia também pode estar presente em crianças prematuras, as quais não possuem o maquinário de utilização de corpos cetônicos pelo cérebro atuando integralmente. Dessa forma, dependem, quase que exclusivamente, da glicose proveniente da glicogenólise e da gliconeogênese hepática, esta última com o ciclo de Cori também limitada naqueles.
Síntese
- Conceito: síntese de-novo de glicose a partir de piruvato;
- Importância: manutenção da glicemia e eliminação de lactato;
- Localização: citosol, principalmente hepático;
- Lógica da via: contorno de conversão irreversível da glicólise (4) e re-síntese (reverso da glicólise); é necessário o transporte mitocondrial de oxalacetato na forma de malato para o citosol;
- Fontes de glicose: propionato (principal), proteína (20-50%, Ala e Gln, principalmente), glicerol, lactato, alfa-cetoácidos;
- Ciclo de Cori: produção de glicose hepática a partir de lactato produzido no músculo;
- Vitaminas necessárias: biotina, niacina (B3, para NADH);
- Consome: NADH, GTP e ATP (em torno de 12 ATPs finais/glicose);
- Regulação: acetil CoA (+), glucagon (+), jejum (+);
- Doença: hipertermia maligna (aumento de processos termogeradores, resultando em quadro de acidose e rigidez muscular).